「コバス® EGFR 変異検出キット v2.0」EGFRチロシンキナーゼ阻害剤(EGFR-TKI)投与前の血漿検査でも保険収載
- ロシュ・ダイアグノスティックス株式会社
- 2017年12月25日
ロシュ・ダイアグノスティックス株式会社(本社:東京都港区/代表取締役社長 兼 CEO:小笠原 信)は、「コバス® EGFR 変異検出キット v2.0」のEGFR-TKI(ゲフィチニブ、エルロチニブ塩酸塩及びアファチニブマレイン酸塩)投与前血漿検査が、12月22日の中央社会保険医療協議会で審議され、2018年1月1日付保険適用が承認されたことをお知らせします。
「コバス® EGFR変異検出キット v2.0」は、ゲノムDNA中のEGFR遺伝子変異を定性的に検出するキットです。非小細胞肺がんの一次治療においてEGFR-TKI治療対象者を層別化する初回検査、およびこれら薬剤に耐性を示す患者に対するEGFR T790M変異検査の際に、それぞれコンパニオン診断薬として用いられます。使用検体は、組織検体および血漿検体が薬事承認されています。
保険適用においては、EGFR-TKI投与前の組織検査、およびEGFR T790M変異検査の組織および血漿検査に対してすでに承認を得ていました。このたびEGFR-TKI投与前の血漿検査に対して保険適用が認められたことで、該当するすべての検査が保険診療で受けられるようになります。血漿検査の保険適用の詳細は以下の通りです。
【保険収載の内容】
測定項目
EGFR 遺伝子検査(血漿)
区分
E3(改良項目)
保険点数
2,100点
測定方法
リアルタイムPCR法
主な測定目的
1.癌組織又は血漿から抽出したゲノムDNA中のEGFR遺伝子変異の検出(ゲフィチニブ、エルロチニブ塩酸塩及びアファチニブマレイン酸塩の非小細胞肺癌患者への適応を判定するための補助に用いる)
2.癌組織又は血漿から抽出したゲノムDNA中のEGFR遺伝子変異(T790M)の検出(オシメルチニブメシル酸塩の非小細胞肺癌患者への適応を判定するための補助に用いる)
留意事項:
1. 本検査は、血漿を用いてリアルタイム PCR 法で測定した場合に算定できる。
2.本検査は、肺癌の詳細な診断及び治療方法を選択する場合、又は肺癌の再発や増悪により、EGFR遺伝子変異の2次的遺伝子変異等が疑われ、再度治療法を選択する場合に、患者1人につきそれぞれの場合で1回に限り算定できる。ただし、本検査の実施は、医学的な理由により、肺癌の組織を検体として、D004-2 悪性腫瘍組織検査 1 悪性腫瘍遺伝子検査 イ EGFR 遺伝子検査(リアルタイムPCR 法)又は ロ EGFR 遺伝子検査(リアルタイムPCR法以外)を行うことが困難な場合に限る。本検査の実施に当たっては、関連学会が定める実施指針を遵守すること。
3.本検査を実施した場合には、肺癌の組織を検体とした検査が実施困難である医学的な理由を診療録及び診療報酬明細書の摘要欄に記載すること。
4.本検査と、肺癌の組織を検体とした D004-2 悪性腫瘍組織検査 1悪性腫瘍遺伝子検査 イ EGFR 遺伝子検査(リアルタイムPCR法)又は ロ EGFR 遺伝子検査(リアルタイムPCR法以外)を同一月中に併せて行った場合には、 主たるもののみ算定する。
【本品の承認および保険適用の範囲】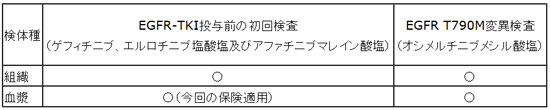
※今回の保険適用承認により、該当するすべての検査が保険診療で受けられるようになります。
【今回の保険適用で対象となるEGFR‐TKI】
アストラゼネカ株式会社の「イレッサ®錠250」(一般名:ゲフィチニブ)
中外製薬株式会社の「タルセバ®錠25mg/タルセバ®錠100mg/タルセバ®錠150mg」(一般名:エルロチニブ塩酸塩)
日本ベーリンガーインゲルハイム株式会社の「ジオトリフ®」(一般名:アファチニブマレイン酸塩)
※その他詳細は掲載元をご覧ください。
- 企業サイトURL
- http://www.roche-diagnostics.jp/
- ニュース・プレスリリース
- http://www.roche-diagnostics.jp/news/17/12/25.html
最新ニュース・プレスリリース
- 【ロシュ・ダイアグノスティックス株式会社】ロシュ・ダイアグノスティックス、質量分析の分野に参入 フルオートメーションの装置で、検査室に革新をもたらす (2025-04-10)
- 【ロシュ・ダイアグノスティックス株式会社】アルツハイマー病の原因となる脳内アミロイドβ濃度を脳脊髄液から調べる検査薬、体外診断用医薬品として製造販売承認を取得 (2025-03-21)
- 【ロシュ・ダイアグノスティックス株式会社】ミスマッチ修復機能欠損判定検査に用いる免疫組織化学染色4項目 子宮体癌患者へのリムパーザ®の投与前検査で保険適用 (2025-02-03)
- 【ロシュ・ダイアグノスティックス株式会社】「ベンタナ OptiView CINtec p16(E6H4)」 子宮頸部上皮内腫瘍の新たな診断補助として保険適用、新発売のお知らせ (2025-01-14)
- 【ロシュ・ダイアグノスティックス株式会社】ロシュ・ダイアグノスティックスとタウンズの取引基本契約に関する基本合意書締結のお知らせ (2024-12-25)


